達格列淨
外觀
 | |||
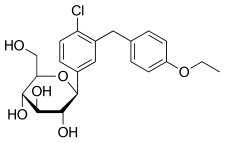 Haworth projection (bottom) | |||
| |||
| 臨床資料 | |||
|---|---|---|---|
| 讀音 | /ˌdæpəɡlɪˈfloʊzɪn/ DAP-ə-glif-LOH-zin | ||
| 商品名 | Forxiga, Farxiga, others | ||
| 其他名稱 | BMS-512148; (1S)-1,5-anhydro-1-C4-chloro-3-[(4-ethoxyphenyl)methyl]phenylD-glucitol | ||
| AHFS/Drugs.com | Monograph | ||
| 核准狀況 |
| ||
| 懷孕分級 | |||
| 給藥途徑 | 口服(錠劑) | ||
| 藥物類別 | SGLT2抑制劑 | ||
| ATC碼 | |||
| 法律規範狀態 | |||
| 法律規範 |
| ||
| 藥物動力學數據 | |||
| 生物利用度 | 78%(投予10毫克劑量後) | ||
| 血漿蛋白結合率 | ~91% | ||
| 藥物代謝 | UGT1A9(主要)、CYP(次要) | ||
| 代謝產物 | Dapagliflozin 3-O-glucuronide(非活性) | ||
| 生物半衰期 | ~12.9 小時 | ||
| 排泄途徑 | 尿 (75%)、糞 (21%)[2] | ||
| 識別資訊 | |||
| |||
| CAS號 | 461432-26-8 | ||
| PubChem CID | |||
| IUPHAR/BPS | |||
| DrugBank | |||
| ChemSpider | |||
| UNII | |||
| KEGG | |||
| ChEBI | |||
| ChEMBL | |||
| CompTox Dashboard (EPA) | |||
| ECHA InfoCard | 100.167.331 | ||
| 化學資訊 | |||
| 化學式 | C21H25ClO6 | ||
| 摩爾質量 | 408.873 | ||
| 3D模型(JSmol) | |||
| |||
| |||
達格列淨(英語:Dapagliflozin,中文品牌名:安達唐(大陸地區)、福適佳(台灣地區), 英文品牌名: Forxiga ), 由阿斯利康研發,是第一種獲批的SGLT2抑制劑,歐盟在2011年首先批准了此藥物。2014年FDA批准其在美國銷售。[3] 達格列淨於2017年獲得中國食品和藥品監督管理總局批准,用於2型糖尿病成人患者改善其血糖控制。[4]
副作用
[編輯]由於達格列淨導致嚴重的糖尿(有時每天約70克),因此可能導致體重迅速減輕和疲倦。 葡萄糖起滲透性利尿劑的作用(這種作用是糖尿病多尿的原因),可導致脫水。 尿液中葡萄糖含量的增加也可能使已經與糖尿病相關的感染惡化,特別是尿路感染及鵝口瘡(念珠菌病)。 極少數情況下,使用SGLT2藥物(包括達格列淨)與會陰壞死性筋膜炎(也稱為Fournier壞疽)有關。[5]
達格列淨也與低血壓反應有關。 人們擔心它可能會增加糖尿病酮症酸中毒的風險。[6]
參考
[編輯]- ^ 1.0 1.1 Dapagliflozin (Farxiga) Use During Pregnancy. Drugs.com. 30 August 2018 [5 May 2020]. (原始內容存檔於2021-04-17).
- ^ 引用錯誤:沒有為名為
Farxiga FDA label的參考文獻提供內容 - ^ Liscinsky, Morgan. FDA approves Farxiga to treat type 2 diabetes. U.S. Food and Drug Administration. Jan 8, 2014 [15 April 2015]. (原始內容存檔於2017-02-17).
- ^ 中国国家食品药品监督管理总局 2017年度药品审评报告. (原始內容存檔於2019-11-06).
- ^ Research, Center for Drug Evaluation and. FDA warns about rare occurrences of a serious infection of the genital area with SGLT2 inhibitors for diabetes. FDA. 9 February 2019 [2019-11-06]. (原始內容存檔於2021-03-08) –透過www.fda.gov.
- ^ Safety Alerts for Human Medical Products — SGLT2 inhibitors: Drug Safety Communication — FDA Warns Medicines May Result in a Serious Condition of Too Much Acid in the Blood. Food and Drug Administration. 15 May 2015 [15 November 2016]. (原始內容存檔於2017-04-06) (英語).

