高铁酸钡
| 高铁酸钡 | |||
|---|---|---|---|

| |||
| |||
| IUPAC名 Barium ferrate(VI) 鐵(VI)酸鋇 | |||
| 别名 | 铁酸钡 | ||
| 识别 | |||
| CAS号 | 13773-23-4 | ||
| SMILES |
| ||
| 性质 | |||
| 化学式 | BaFeO4 | ||
| 摩尔质量 | 257.1646 g·mol⁻¹ | ||
| 外观 | 深红色晶体 | ||
| 溶解性(水) | 不溶 | ||
| 结构 | |||
| 晶体结构 | 正交晶系 | ||
| 空间群 | Pnma, No. 62[1] | ||
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |||
高铁酸钡是一种无机化合物,化学式 BaFeO4。它是一种罕见的六价铁化合物。[2] 其中的铁(VI)酸根离子有两个不成对电子,所以是顺磁性的。[3]它的结构类似BaSO4,含有四面体型的[FeO4]2− 阴离子。[4]
结构
[编辑]其中的高铁酸根阴离子是顺磁性的,因为它有两个不成对电子,而且是四面体形分子构型的。[3]
X射线晶体学显示BaFeO4 纳米晶是正交晶系的[1](晶格参数 a ≠ b ≠ c,α=β=γ=90°)[5]。它的空间群为 Pnma,晶格参数 a = 0.8880 nm、b = 0.5512 nm 和c = 0.7214 nm。[1]
表征
[编辑]在 870、812、780 cm−1处都观察到高铁酸钡的红外吸收峰。[6]
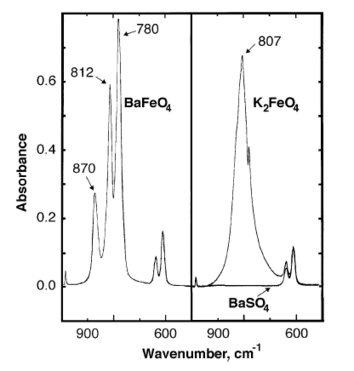
BaFeO4 遵守居里-外斯定律,磁矩为 (2.92 ± 0.03) × 10−23 A m2 (3.45 ± 0.1 BM),外斯参数为 −89 K。[8]
制备和反应
[编辑]高铁酸钡可以通过干法或湿法制备。干法合成通常会加热,[6]例如氢氧化钡和氢氧化亚铁在氧气存在下加热到 800 至 900 °C而成。[9]
- Ba(OH)
2 + Fe(OH)
2 + O
2 → BaFeO
4 + 2 H
2O
湿法则采用化学和电化学技术。举个例子,当将氢氧化铁置于碱性条件下并加入强氧化剂(如次氯酸钠)时,就会形成高铁酸根阴离子。[10]
- 2 Fe(OH)
3 + 3 OCl−
+ 4 OH−
→ 2 FeO2−
4 + 5 H
2O + 3 Cl−
在溶液中加入钡盐,得到高铁酸钡沉淀。[10]将可溶的钡盐加入到碱金属高铁酸盐溶液中,会产生深红色的高铁酸钡沉淀。这种晶体有和铬酸钡一样的结构,溶解度也差不多。[11]高铁酸钡也可以由氧化钡加到次氯酸钠和硝酸铁的混合物中而成。[12]通过在没有二氧化碳的情况下低温进行反应,并通过快速过滤和干燥沉淀物,减少氢氧化钡和碳酸钡作为杂质共沉淀,可以提高产品的纯度。[11]
用处
[编辑]高铁酸钡是一种氧化剂,可用于有机合成。它也用于脱色、去除氰化物、杀灭细菌以及污染和废水的处理。[6]
高铁酸盐可作为“超级铁”电池的高能阴极材料。含有高铁酸盐的阴极因为高度氧化、多电子转移和高内能,而被称为“超级铁”阴极。在所有高铁酸盐中,高铁酸钡的电荷转移异常容易,这对于碱性电池的高功率领域很重要。[7]
参见
[编辑]参考资料
[编辑]- ^ 1.0 1.1 1.2 Ni, Xiao-Min; Ji, Ming-Rong; Yang, Zhi-Ping; Zheng, Hua-Gui. Preparation and structure characterization of nanocrystalline BaFeO4. Journal of Crystal Growth. 2004, 261 (1): 82–86. doi:10.1016/j.jcrysgro.2003.09.024.
- ^ Briggs, J. G. R. Longman A-level course in chemistry 4th. Pearson Education South Asia. 2005: 536. ISBN 978-981-4105-08-8.
- ^ 3.0 3.1 Wiberg, Egon; Wiberg, Nils; Holleman, Arnold. Inorganic chemistry. Academic Press. 2001: 1457–1458. ISBN 978-0-12-352651-9.
- ^ Wells, A.F. Structural inorganic chemistry 5th. Oxford [Oxfordshire]: Clarendon Press. 1986. ISBN 978-0-19-855370-0.
- ^ IUCr. www.iucr.org. [2016-04-29]. (原始内容存档于2021-07-21).
- ^ 6.0 6.1 6.2 Henry-Chase, Adonica; Bhushan Tewari, Brij. Use to Ferrate (VI) A Green Chemical for the Environment Remediation (PDF). Revista Boliviana de Química. 2013, 30 (1): 13–23 [2021-07-21]. ISSN 0250-5460. (原始内容存档 (PDF)于2019-11-04).
- ^ 7.0 7.1 Licht, Stuart; Naschitz, Vera; Wang, Baohui. Rapid chemical synthesis of the barium ferrate super-iron Fe (VI) compound, BaFeO4. Journal of Power Sources. 2002, 109: 67–70. doi:10.1016/s0378-7753(02)00041-1.
- ^ Audette, R. J.; Quail, J. W. Potassium, rubidium, cesium, and barium ferrates(VI). Preparations, infrared spectra, and magnetic susceptibilities. Inorganic Chemistry. 1972, 11 (8): 1904–1908. doi:10.1021/ic50114a034.
- ^ Sharma, R. K. Stabilisation of Fe (VI). Textbook of Coordination Chemistry. New Delhi: Discovery Publishing House. 2007: 124 [2021-07-21]. ISBN 9788183562232. (原始内容存档于2021-07-21).
- ^ 10.0 10.1 Wulfsberg, Gary. pH and the stability of high oxidation states; Syntheses of oxo anions and their use as oxidizing agents. Principles of Descriptive Inorganic Chemistry. Sausalito, CA: University Science Books. 1991: 142–143 [2021-07-21]. ISBN 9780935702668. (原始内容存档于2021-07-21).
- ^ 11.0 11.1 Gump, J. R.; Wagner, W. F.; Schreyer, J. M. Preparation and analysis of barium ferrate(VI). Analytical Chemistry. 1954, 26 (12): 1957. ISSN 0003-2700. doi:10.1021/ac60096a027.
- ^ Herber, Rolfe H.; Johnson, David. Lattice dynamics and hyperfine interactions in M2FeO4 (M = K+, Rb+, Cs+) and M'FeO4 (M' = Sr2+, Ba2+). Inorganic Chemistry. 1979, 18 (10): 2786–2790. doi:10.1021/ic50200a030.


