硫化鉀
外觀
| 硫化鉀 | |
|---|---|
| |

| |
| IUPAC名 Potassium sulfide | |
| 識別 | |
| CAS號 | 1312-73-8 |
| PubChem | 162263 |
| ChemSpider | 142491 |
| SMILES |
|
| RTECS | TT6000000 |
| 性質 | |
| 化學式 | K2S |
| 摩爾質量 | 110.262 g·mol⁻¹ |
| 外觀 | 無色晶體 不純時為黃棕色的固體 |
| 密度 | 1.8 g/cm3 |
| 熔點 | 840 °C |
| 溶解性(水) | 水解為KSH、KOH |
| 溶解性(其他溶劑) | 可溶於乙醇和甘油 |
| 結構 | |
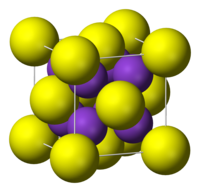
| 晶體結構 | 反螢石型結構 |
| 危險性 | |
| 警示術語 | R:R31, R34 |
| 安全術語 | S:S26, S45 |
| 主要危害 | 有毒 |
| 相關物質 | |
| 其他陰離子 | 氧化鉀 硒化鉀 碲化鉀 釙化鉀 |
| 其他陽離子 | 硫化鈉、硫化銣、硫化銫、硫化鈁 |
| 若非註明,所有數據均出自標準狀態(25 ℃,100 kPa)下。 | |
硫化鉀是一個無機鹽類,化學式為K2S。它的晶體結構與硫化鋰、硫化鈉和硫化銣類似,都為反螢石型結構,半徑較小的鉀離子占CaF2中的F−位,較大的硫離子佔八配位的Ca2+位。[1]
硫化鉀與其他鹼金屬硫化物類同,[1] 含有強鹼性的S2−陰離子,溶於水時強烈水解為氫氧化鉀和硫化氫鉀:
- K2S + H2O → KOH + KSH
實際中通常不需考慮該反應,含SH−與OH−的混合溶液可以作S2−來源。
K2S可由單質鉀與硫化合製備。該反應十分劇烈,實驗室中常以液態的無水氨作介質。
多硫化鉀(K2Sx)是多硫化物的一類,含有多硫離子Sx2−,可由硫溶於硫化鉀溶液製備。其顏色隨着x值增大而加深,與酸反應放出硫化氫氣體,多餘的硫沉澱下來。
參考資料
[編輯]- ^ 1.0 1.1 Holleman, A. F.; Wiberg, E. "Inorganic Chemistry" Academic Press: San Diego, 2001. ISBN 0-12-352651-5.
