亚急性硬化性全脑炎
外观
(重定向自亚急性硬化性泛脑炎)
亞急性硬化性全腦炎(英語:Subacute sclerosing panencephalitis, SSPE) 是一種感染麻疹病毒後的腦炎併發症,是一種會致命、漸進性,造成中樞神經廣泛去髓鞘的慢性中樞神經退化性疾病,通常在感染麻疹病毒後7到10年發生。
流行病學
[编辑]- 1960~1974年間,每百萬被麻疹病毒感染的人中有8.5個人會有SSPE風險;在 1970 到 1980 年間,因爲廣泛接受疫苗接種,SSPE風險降低到百萬被麻疹病毒感染的人中0.06人。[1]
- 在1989到1991年間,美國的麻疹病毒感染興起,SSPE風險增為 200/百萬人。[2]
- 以下是各國發生率的資料:(單位:個案數/百萬人)
- SSPE好發於 20 歲以前,通常是感染麻疹病毒後 7 到 10 年發生。[2]
- SSPE的風險因子包括「麻疹發病年齡小」、「居住在鄉村地區」、「貧窮環境」,以及有先天性免疫缺乏症的患者,或是兒子的母親有先天性免疫缺乏症等等。[6]
- 小時感染麻疹病毒是 SSPE 的風險因子之一,大約有一半數量的SSPE患者都在兩歲之前就感染麻疹病毒。
- 因為小孩免疫系統尚不成熟,接觸麻疹病毒的年齡越早(不包括麻疹疫苗),發展為SSPE的可能性就越大。
- 有接受麻疹疫苗的人,其得到SSPE的風險比沒有接受疫苗者高。
- 雖然接受麻疹疫苗,也可以說是接受了麻疹病毒,但不致造成SSPE,所以接受麻疹疫苗非SSPE的致病風險。[6]
- 在正常的免疫系統中,感染麻疹病毒後,麻疹病毒會促發細胞介導免疫,包括活化T-helper 1細胞(Th1)、釋放干擾素-ɑ(INF-ɑ)和 IL-2,以從被感染細胞中清除病毒。[7]
- 因此,如果細胞介導免疫反應不全,便無法有效清除被感染細胞,寄留在體內。
- 接著,麻疹病毒會利用CD46和protein F等蛋白質進入神經系統。
- CD9可能也扮演重要角色,使得可以 SSPE 患者的CSF裡檢驗到高濃度抗CD9抗體。
- 一旦麻疹病毒進入細胞內,病毒會改變細胞蛋白質避免被免疫系統辨識出,以及在細胞內繁殖時又不至於讓細胞變化太多,避免破壞宿主神經元。
- 在臨床表現上變明顯之前,麻疹病毒可以在細胞中保持休眠數年,但最中病毒會引發針對被感染細胞的發炎反應,導致廣泛的中樞神經系統受損。
分期
[编辑]- 第一期:人格變化、嗜睡、學習困難和行為異常,可能持續數週到數年。
- 第二期:肌躍症(myoclonus,每五到十秒發生一次)、失智惡化、長距離運動與感覺疾病,這階段通常持續3~12個月。
- 第三期:肌肉鬆弛(Flaccidity)、皮質僵硬(Decorticate rigidity )、肌躍症消失以及自主神經功能紊亂的症狀和徵兆。
- 第四期:持續性植物狀態(Persistent vegetative state),俗稱植物人,通常死亡會發生在這階段(但死亡在每一階段都可能會發生[9])。
- 每人病人的進展速度不同,有些人很快就從一期到下一期,有些人則停留在某一期一段時間。[10])
- 癲癇在每一階段都可能發生。
診斷
[编辑]
EEG
[编辑]- 65~83%的SSPE患者可在腦波圖上看到週期性的複合波,通常發生在睡眠時期。[6]
- 在第二期,腦波圖會顯示突發高電壓(300~500 微伏特),頻率 2~3 秒的delta波和尖波組成的復合物,此復合波每 3~20 秒出現一次,每次持續 0.5~3 秒,每個複合波之後會伴隨相對較平坦的波形。
MRI
[编辑]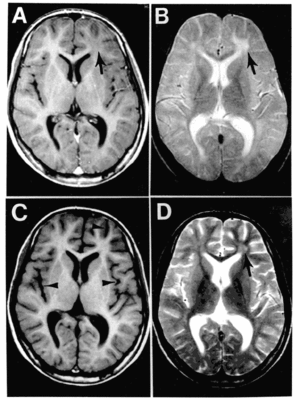
- 右圖說明中的T1-weighted和T2-weighted,詳細說明需物理基礎,臨床上,T1大多是看解剖構造,T2會把異常訊號放大,那異常之處顯得清楚可見,因此常看「病理」。可以發現圖AC都是T1,顏色差異不大,BD都是T2,顏色分明,容易看到異常之處。
其他
[编辑]- 頭部CT掃描可見萎縮和疤痕
- F-fluorodeoxyglucose(氟-18去氧葡萄糖)正子攝影和核磁頻譜可見大腦功能異常,可作為 SSPE 早期診斷和評估 SSPE 早期對特定大腦功能造成的影響。
| 主要標準 | 次要標準 |
|---|---|
- 快速發展的失智症
- 肌躍症(myoclonus)
- 癲癇
- 急性瀰漫性腦脊髓炎(Acute disseminated encephalomyelitis, ADEM)
- 急性病毒性腦炎
- 腫瘤
- 多發性硬化症
- 代謝性白質疾病
- 慢性Rasmussen腦炎
- Unverricht–Lundborg disease
- Lafora disease
- 青少年型神經元蠟樣脂褐質沈積病(Juvenile ceroid lipofuscinosis, JNCL)
- myoclonic epilepsy with red ragged fibres
- 神經氨酸酶缺乏症
- 沒有有效治療方法
- 若病人還在第一期,可以使用isoprinosine (页面存档备份,存于互联网档案馆)或是腦室內給予Interferon-ɑ,但藥物的療效在每個病人上不一樣
- 每週腦室內給予Interferon-ɑ
- 每日口服Isoprinosine
- 以上兩藥可以組合一起使用
- 支持性療法
參考資料
[编辑]- Hayley Gans, Yvonne A Maldonado. (2018). Measels: Clinical manifestations, diagnosis, treatment, and prevention. In Meg Sullivan. (Ed.). Retrieved October 9, 2019, from https://www-uptodate-com.autorpa.mmh.org.tw/contents/measles-clinical-manifestations-diagnosis-treatment-and-prevention
- ^ Centers for Disease. Subacute sclerosing panencephalitis surveillance-United States. Morbidity and Mortality Weekly Report. 1982, 5 (31): 585–588. PMID 6817063.
- ^ 2.0 2.1 Bellini, W.J.; Rota, J.S.; Lowe, L.E.; Katz, RS; Dyken ., P.R.; Zaki, S.R.; Shieh, W.J.; Rota, P.A. Subacute sclerosing panencephalitis: More cases of this fatal disease are prevented by measles immunization than was previously recognized. The Journal of Infectious Disease. 2005, 192 (10): 1686–1693. PMID 16235165. doi:10.1086/497169.
- ^ 3.0 3.1 Campbell, H..; Andrews, N..; Brown, K.E..; Miller, E. Review of the effect of measles vaccination on the epidemiology of SSPE.. International Journal of Epidemiology. 2007, 36 (6): 1334–1348. PMID 18037676. doi:10.1093/ije/dym207.
- ^ Campbell, C.; Levin, S.; Huphreys, P.; Walop, W.; Brannan, R. Subacute sclerosing panencephalitis: results of the Canadian Paediatric Surveillance Program and review of the literature.. BMC Pediatrics. 2005, 5 (47). PMID 16356180. doi:10.1186/1471-2431-5-47.
- ^ Singer, C.; Lang, A.E.; Suchowersky, O. Adult-onset subacute sclerosing panencephalitis: case reports and review of the literature. Movement Disorders. 1997, 12 (3). PMID 9159729. doi:10.1002/mds.870120313.
- ^ 6.00 6.01 6.02 6.03 6.04 6.05 6.06 6.07 6.08 6.09 6.10 Gutierez, Jose; Issacson, R.S.; Koppel, B.S. Subacute sclerosing panencephalitis: an update. Development Medicinal & Child Neurology. 2010, 52 (10): 901–907. PMID 20561004. doi:10.1111/j.1469-8749.2010.03717.x.
- ^ 7.0 7.1 Griffin, D.E.; Ward, B.J.; Esolen, L.M. Pathogenesis of measles virus infection: an hypothesis for altered immune responses. The Journal of Infectious Diseases. 1994: s24–s31. PMID 7930750. doi:10.1093/infdis/170.supplement_1.s24.
- ^ Inoue, T.; Kira, R.; Nakao, F.; Ihara, K.; Bassuny, W.M.; Kusuhara, K.; Nihei, K.; Takeshita, K.; Hara, T. PContribution of the interleukin 4 gene to susceptibility to subacute sclerosing panencephalitis. Arch Neurol. 2002, 59 (2): 822–827. PMID 12020266. doi:10.1001/archneur.59.5.822.
- ^ Garg, R.K. Subacute sclerosing panencephalitis. Journal of Neurology. 2008, 255 (12): 1861–1871. PMID 18846316. doi:10.1007/s00415-008-0032-6.
- ^ Liko, J.; Guzman-Cottrill, J.A.; Cieslak, P.R. Notes from the Field: Subacute Sclerosing Panencephalitis Death - Oregon, 2015.. Morbidity and Mortality Weekly Report. 2016, 65 (1): 10–11. PMID 26765654. doi:10.15585/mmwr.mm6501a3.
外部連結
[编辑]- 23-273l. at Merck Manual of Diagnosis and Therapy Home Edition
- 美國國家神經疾病及中風研究院上有關subacute_panencephalitis的資料
- PubMed Health: Subacute sclerosing panencephalitis(页面存档备份,存于互联网档案馆)
- synd/1889 - Who Named It?
